Acidi, Esteri e Lattoni.
Derivati degli acidi carbossilici
I principali acidi mono-, bi-, e tricarbossilici presenti nei vini:
Lattoni:
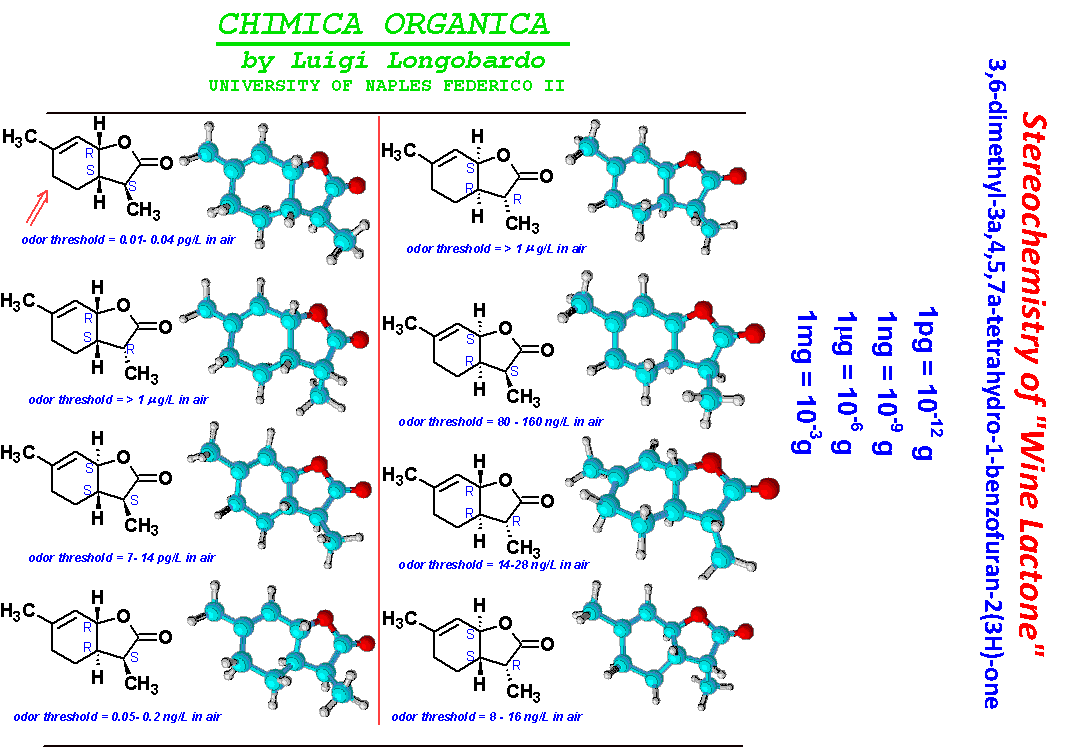
Quando la funzione alcolica è essa stessa presente nella struttura dell'acido carbossilico si forma un estere ciclico, che prende il nome di lattone:
Per una discussione generale sul "wine Lacton" vedi:
http://fco0809.blogspot.com/2009/05/lezione-del-6-maggio-2009.htmlDerivati degli acidi carbossilici:
Si definiscono derivati degli acidi carbossilici tutte quelle sostanze che per idrolisi (reazioni con H2O, catalizzate da acidi o basi) forniscono i corrispondenti acidi carbossilici. Tra essi, gli alogenuri acilici e le anidridi sono troppo reattive e pertanto non si trovano in natura. A differenza degli alogenuri alchilici, dove l'atomo di alogeno è legato ad un carbonio sp3, negli alogenuri acilici l'alogeno è legato direttamente al carbonio carbonilico ibridato sp2: