ACIDI NUCLEICI
Confronto tra piridina e pirrolo. La piridina è una sostanza basica mentre il pirrolo non lo è, anche se entrambe contengono un azoto ibridato sp2. Richiamo del concetto di aromaticità.
Pirimidina e imidazolo. Composti eterociclici a 6 e 5 termini contenenti 2 atomi di azoto. Imidazolo: proprietà acide e basiche.
Prodotti ottenuti dall'idrolisi degli acidi nucleici:
RNA: H3PO4 + D-ribosio + miscela di basi eterocicliche: adenina (A), uracile (U), citosina (C), guanina (G).
DNA: H3PO4 + 2-deossi-D-ribosio + miscela di basi eterocicliche: adenina, timina (T), citosina, guanina.
Struttura degli acidi nucleici: Nucleosidi e Nucleotidi.
Polinucleotidi: I nucleotidi sono condensati attraverso la formazione di esteri fosforici a ponte tra l'ossidrile 5' di un anello furanosico e l'ossidrile 3' di un altro anello. Formazione di legami ad idrogeno tra la A e la T e tra la G e la C. La doppia elica del DNA. Duplicazione di una molecola di DNA.
Trascrizione e traduzione del codice genetico; il dogma della biologia molecolare: il DNA fa l'RNA e l'RNA fa le proteine.
Approfondimenti in
http://fco0809.blogspot.it/2009/05/lezione-del-5-maggio-2009.html

AAC – AMINO ACIDS CHEMISTRY DEPARTMENT OF CHEMICAL SCIENCES AT UNINA Dr. Luigi Longobardo • Room 2N19; Lab 2N18ab; • phone +39-081-674115; • Email: luilongo@unina.it; luilongo@gmai.com • orcid • webdocenti • Group website: http://fco0809.blogspot.it/ Research: Asymmetric synthesis Synthetic manipulation of α-amino acids. Sulfur and selenium-containing unnatural amino acids. Chemistry of Hydroxycinnamic Acids.
7 mag 2012
25 apr 2012
Lezione del 24 aprile 2012
Amminoacidi, peptidi e proteine
Le lezioni riprenderanno lunedì 7 maggio 2012 alle ore 9.00
Amminoacidi: definizioni e classificazioni. alfa, beta e gamma amminoacidi. Amminoacidi naturali e i 20 amminoacidi proteinogenici. Stereochimica: serie steriche. L e D amminoacidi. Correlazioni con la stereochimica assoluta.
Catene laterali degli amminoacidi proteinogenici: Gli amminoacidi essenziali. Amminoacidi polari e apolari. Proprietà acido-base. definizione di punto isoelettrico. Calcolo del punto isoelettrico di glicina, acido aspartico e lisina.
La formazione di peptidi. Condensazione tra le funzione carbossilica e quella amminica. Formazione di ammidi. Il caso Alanina + Glicina. I 4 dipeptidi possibili:
Ala-Gly; Gly-Ala; Ala-Ala; Gly-Gly. I dipeptidi Ala-Gly e Gly-Ala sono tra loro isomeri strutturali.
Proteine. Strutture primarie. Cenni di strutture secondarie e terziarie. Relazione tra numero di amminoacidi da condensare e la lunghezza delle catene peptiche e proteiche. Spazi proteici possibili e spazi proteici reali. L'evoluzione dei sistemi biologici.
Approfondimenti in :
http://fco0809.blogspot.it/2009/05/lezione-del-29-aprile-2009.html
Le lezioni riprenderanno lunedì 7 maggio 2012 alle ore 9.00
Le lezioni riprenderanno lunedì 7 maggio 2012 alle ore 9.00
Amminoacidi: definizioni e classificazioni. alfa, beta e gamma amminoacidi. Amminoacidi naturali e i 20 amminoacidi proteinogenici. Stereochimica: serie steriche. L e D amminoacidi. Correlazioni con la stereochimica assoluta.
Catene laterali degli amminoacidi proteinogenici: Gli amminoacidi essenziali. Amminoacidi polari e apolari. Proprietà acido-base. definizione di punto isoelettrico. Calcolo del punto isoelettrico di glicina, acido aspartico e lisina.
La formazione di peptidi. Condensazione tra le funzione carbossilica e quella amminica. Formazione di ammidi. Il caso Alanina + Glicina. I 4 dipeptidi possibili:
Ala-Gly; Gly-Ala; Ala-Ala; Gly-Gly. I dipeptidi Ala-Gly e Gly-Ala sono tra loro isomeri strutturali.
Proteine. Strutture primarie. Cenni di strutture secondarie e terziarie. Relazione tra numero di amminoacidi da condensare e la lunghezza delle catene peptiche e proteiche. Spazi proteici possibili e spazi proteici reali. L'evoluzione dei sistemi biologici.
Approfondimenti in :
http://fco0809.blogspot.it/2009/05/lezione-del-29-aprile-2009.html
Le lezioni riprenderanno lunedì 7 maggio 2012 alle ore 9.00
23 apr 2012
Lezione del 23 aprile 2012
Carboidrati
Formazione dei carboidrati in natura. Gliceraldeide. Serie steriche.
D e L-gliceraldeide. D-Tetrosi: D-Eritrosio e D-Treosio. D-Aldopentosi.
D-Ribosio. Processi di emiacetalizzazione in soluzione acquosa:
Glicosidi. Formazione di O,O-acetali misti con alcoli, ROH. Formazione di di-tri..polisaccaridi.
Formazione di O,N-acetali, cioè di N-Glicosidi. Nucleosidi. RNA e DNA.
La freccia del tempo in Fisica e in Chimica.
Vedi anche :
http://fco0809.blogspot.it/2009/05/lezione-del-28-aprile-2009.html
Formazione dei carboidrati in natura. Gliceraldeide. Serie steriche.
D e L-gliceraldeide. D-Tetrosi: D-Eritrosio e D-Treosio. D-Aldopentosi.
D-Ribosio. Processi di emiacetalizzazione in soluzione acquosa:
Glicosidi. Formazione di O,O-acetali misti con alcoli, ROH. Formazione di di-tri..polisaccaridi.
Formazione di O,N-acetali, cioè di N-Glicosidi. Nucleosidi. RNA e DNA.
La freccia del tempo in Fisica e in Chimica.
Vedi anche :
http://fco0809.blogspot.it/2009/05/lezione-del-28-aprile-2009.html
18 apr 2012
Lezione del 17 aprile 2012
Lezione: Reattività del gruppo carbonilico. Ibridazione e geometria. Idratazione dell'acetaldeide e dell'acetone. La formazione dei composti carbonilici in natura. Fotosintesi clorofilliana. Gliceraldeide. Il lavoro di Fischer e la stereochimica relativa. Proiezioni. Serie steriche. Correlazione tra stereochimica relativa e stereochimica assoluta. D-Aldotreosi. D-Aldopentosi.
Esercitazione: La reattività dei composti carbonilici con gli alcoli. Processi di acetalizzazione acido catalizzati. La reazione tra acetaldeide e metanolo.
D-aldoesosi. Glucosio, Mannosio e galattosio. Formazioni di emiacetali ciclici.
alfa e beta anomeri. Mutarotazione.
Vedi anche
http://fco0809.blogspot.it/2009/04/lezione-del-22-aprile-2009.html
Esercitazione: La reattività dei composti carbonilici con gli alcoli. Processi di acetalizzazione acido catalizzati. La reazione tra acetaldeide e metanolo.
D-aldoesosi. Glucosio, Mannosio e galattosio. Formazioni di emiacetali ciclici.
alfa e beta anomeri. Mutarotazione.
Vedi anche
http://fco0809.blogspot.it/2009/04/lezione-del-22-aprile-2009.html
16 apr 2012
Lezione del 16 aprile 2012
Acidi Carbossilici e derivati. Processi di esterificazione. Meccanismo della reazione. Come influenzare un processo di equilibrio. Il caso del Fe(OH)3.
Processi di esterificazione intramolecolari. Formazione di Lattoni. Whisky lactone e Wine lactone. Soglie di percezione. Acidità degli acidi carbossilici. Come la presenza di atomi o gruppi di atomi elettron-attrattori influenza l'acidità. Il caso dell'acido trifluoroacetico, CF3COOH.
Separazione di una miscela di sostanze organiche sfruttando le loro proprietà acido-base (RCOOH + R'CH2OH + R''-NH2).
Per approfondimenti vedi:
http://fco0809.blogspot.it/2009/03/lezione-del-24-marzo-2009.html
http://fco0809.blogspot.it/2010/03/acidi-esteri-e-lattoni-30-marzo-2010.html
http://fco0809.blogspot.it/2009/04/lezione-del-21-aprile-2009.html
Processi di esterificazione intramolecolari. Formazione di Lattoni. Whisky lactone e Wine lactone. Soglie di percezione. Acidità degli acidi carbossilici. Come la presenza di atomi o gruppi di atomi elettron-attrattori influenza l'acidità. Il caso dell'acido trifluoroacetico, CF3COOH.
Separazione di una miscela di sostanze organiche sfruttando le loro proprietà acido-base (RCOOH + R'CH2OH + R''-NH2).
Per approfondimenti vedi:
http://fco0809.blogspot.it/2009/03/lezione-del-24-marzo-2009.html
http://fco0809.blogspot.it/2010/03/acidi-esteri-e-lattoni-30-marzo-2010.html
http://fco0809.blogspot.it/2009/04/lezione-del-21-aprile-2009.html
7 apr 2012
Risultati test in itinere del 3 aprile 2012
| 123 | …………….. | 18 | ||
| 181 | …………….. | 18 | ||
| 185 | …………….. | 16 | ||
| 186 | ……………… | 24 | ||
| 187 | ……………… | 12 | * identico al 211 | |
| 188 | ……………… | 6 | ||
| 191 | ……………… | 10 | ||
| 192 | ……………… | 24 | ||
| 193 | ……………… | 20 | ||
| 194 | ………………. | 18 | ||
| 195 | ………………. | 25 | ||
| 197 | ………………. | 18 | ||
| 200 | ………………. | 18 | ||
| 201 | ………………. | 6 | ||
| 202 | ……………… | 20 | ||
| 204 | ……………… | 22 | ||
| 205 | …………….. | 18 | ||
| 208 | ……………… | 18 | ||
| 210 | ……………… | 18 | ||
| 211 | ……………… | 12 | * identico al 187 | |
| 212 | ……………… | 18 | ||
| 214 | ………………. | 19 | ||
| 216 | ………………. | 10 | ||
| 217 | ………………. | 6 | ||
| 219 | ………………… | 16 | ||
| 220 | ………………… | 18 | ||
| 222 | ……………….. | 16 | ||
| 224 | ………………. | 10 | ||
4 apr 2012
Test in itinere del 3 aprile 2012
 |
Università degli Studi di
Napoli Federico II
Test
in itinere
03
aprile 2012
Nome_____________________________________
Matricola___________________________________
|
1. Per l’idrocarburo eptano (C7H16) è possibile
prevedere l’esistenza di nove isomeri
strutturali. In realtà esistono complessivamente undici isomeri, includendo tra essi anche i possibili
stereoisomeri. Provare a scrivere qualche isomero, attribuendo loro il nome.
2. Scrivere le strutture e
attribuire i nomi a tutti i possibili propandioli (C3H8O2),
oppure butandioli (C4H10O2), oppure
pentandioli (C5H12O2).
3.
Assegnare il nome
completo alle molecole di seguito indicate:
4. Indicare molecole
appartenenti alle seguenti classi, fornendo almeno un esempio per ogni classe e
attribuendo loro i rispettivi nomi: a) acidi carbossilici; b) chetoni; c)
eteri; d) dieni isolati; e) aldeidi; f) esteri; g) ammine secondarie; h)
ammidi.
5. Fornire, spiegando brevemente, esempi di strutture molecolari utili
a definire i seguenti concetti: a) ibridazione; b) configurazione e
conformazione; c) risonanza; d) enantiomeri e diastereoisomeri; e) acidità.
2 apr 2012
Lezione del 2 aprile 2012
Argomenti di ricapitolazione:
Ibridazione del Carbonio. Alcani. Alcheni. Geometria E/Z. Alchini. Dieni isolati e dieni coniugati. Idrocarburi aromatici. Benzene. Il concetto di risonanza. Regole per attribuire l'aromaticità ad una molecola. Alcoli. Eteri. Stereochimica. Enantiomeri e diastereoisomeri. Regola 2 alla n.
Assegnazione della configurazione assoluta ad un carbonio asimmetrico. Composti carbonilici. Aldeidi e chetoni. Nonanale, Chanel N°5. Acidi carbossilici e derivati. Esteri. Formiato di etile, un babà al rum. Composti contenenti azoto. Ammine e ammidi.
Reattività. Addizione di acidi alogenidrici agli alcheni. Regola di Markovnikov. Addizione di HX ai dieni coniugati. Addizione 1,2 e 1,4.
Ibridazione del Carbonio. Alcani. Alcheni. Geometria E/Z. Alchini. Dieni isolati e dieni coniugati. Idrocarburi aromatici. Benzene. Il concetto di risonanza. Regole per attribuire l'aromaticità ad una molecola. Alcoli. Eteri. Stereochimica. Enantiomeri e diastereoisomeri. Regola 2 alla n.
Assegnazione della configurazione assoluta ad un carbonio asimmetrico. Composti carbonilici. Aldeidi e chetoni. Nonanale, Chanel N°5. Acidi carbossilici e derivati. Esteri. Formiato di etile, un babà al rum. Composti contenenti azoto. Ammine e ammidi.
Reattività. Addizione di acidi alogenidrici agli alcheni. Regola di Markovnikov. Addizione di HX ai dieni coniugati. Addizione 1,2 e 1,4.
28 mar 2012
Lezione del 27 marzo 2012
Alcheni, dieni, polieni e composti aromatici
Lezione:
Vedi anche:
http://fco0809.blogspot.it/2009/04/lezione-del-6-aprile-2009.html
http://fco0809.blogspot.it/2009/04/lezione-del-7-aprile-2009.html
Esercitazione:
Lezione:
Addizione di acidi alogenidrici. Idrogenazione. Addizione Syn. Stereoselettività. Addizione di alogeni: addizione anti. Conseguenze stereochimiche. Dieni isolati e dieni coniugati Addizioni di acidi alogenidrici ai dieni coniugati. Idrogenazione dei polieni ciclici. Cicloesene, 1,3 -cicloesadiene e 1,3,5-cicloesatriene. Confronto tra i calori di idrogenazione. Benzene. Risonanza. Composti Aromatici. Regole per attribuire il carattere aromatico alle molecole organiche.
Vedi anche:
http://fco0809.blogspot.it/2009/04/lezione-del-6-aprile-2009.html
http://fco0809.blogspot.it/2009/04/lezione-del-7-aprile-2009.html
Esercitazione:
Analisi delle tracce di precedenti prove scritte. Nomenclatura dei composti aromatici. Fenoli. Confronto tra l'acidità del fenolo e quella del cicloesanolo.
Incremento di acidità dovuto alla presenza di gruppi elettron-attrattatori e stabilizzazione per risonanza degli ioni fenato. 2,4,6-trinitrofenolo. Pirati e uso dell'acido picrico. Nascita del tritolo.
26 mar 2012
Lezione del 26 marzo 2012
Il concetto di risonanza
Lo ione carbonato. Equivalenza dei legami C-O. La struttura reale è descrivibile tramite tre formule di risonanza isoenergetiche.
Confronto della proprietà acido-base tra l'acido acetico (pKa = 5) e l'etanolo (pKa = 15). Stabilizzazione per risonanza dello ione carbossilato.
Ammine e Ammidi. Assenza di basicità e stabilizzazione per risonanza delle ammidi. Il confronto tra Etilammina e Acetammide. Conseguenze biochimiche.
Vedi anche fco0809.blogspot.it/2009/03/lezione-del-24-marzo-2009.html
Vedi anche fco0809.blogspot.it/2009/03/lezione-del-24-marzo-2009.html
Addizione di acidi alogenidrici agli alcheni. Carbocationi primari, secondari e terziari. Regola di Markovnikov.
21 mar 2012
Lezione del 20 marzo 2012
Stereochimica
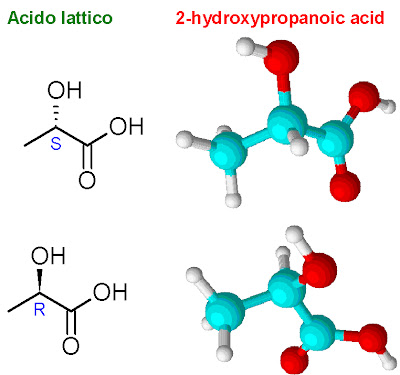
Lezione: Carboni asimmetrici. Ancora sui due acidi lattici. Regole CIP per assegnare la configurazione assolute. Enantiomeri R e S. Molecole con due centri chirali. Regola 2 alla n. I quattro pentan-2,3-dioli. Configurazioni assolute. Enantiomeri e diastereoisomeri. Gli enantiomeri del 2-butanolo.
Butan-2,3-dioli. Presenza di un piano di simmetria. Riduzione del numero complessivo di stereoisomeri. Molecole organiche contenenti carboni asimmetrici che non sono chirali. Le Meso-forme. Gli acidi Tartarici (acidi 2,3-diidrossibuntandioici)
Esercitazioni: Una coppia di enantiomeri delle otto possibili presenti nell'acido 5-ammino-2-bromo-3-cloro-4-idrossiesanoico. Assegnazione di tutte le configurazioni assolute.
La Stereochimica nelle molecole cicliche. Ancora sugli 1,2-dimetilciclopropani.
Limoneni. S ed R-limoneni: assegnazione delle configurazioni assolute.
Limoneni. S ed R-limoneni: assegnazione delle configurazioni assolute.
Valutazioni odorose del R-limonene (arancio) e dell'S-limonene (limone) presenti in una soluzione alcolica.
19 mar 2012
Lezione del 19 marzo 2012
Introduzione alla stereochimica.
Luce ordinaria e luce polarizzata. Polarimetro. Evidenze sperimentali: sostanze naturali che ruotano il piano della luce polarizzata. Stereoisomeria. Il carbonio tetraedrico (sp3) legato a 4 atomi o 4 gruppi di atomi diversi. Oggetti chirali e oggetti non chirali. Simmetria. I due acidi lattici. Modelli tridimensionali. La necessità di rappresentate in 2D le molecole reali (3D). Modelli a cuneo pieno e tratteggiato. I 16 possibili stereoisomeri dell'acido 5-ammino-2-bromo-3-cloro-4-idrossiesanoico. I progressi della Chimica e il proliferare delle scienze molecolari.
14 mar 2012
Lezione del 13 marzo 2012
Lezione: Molecole contenenti C, H, O. Alcoli. Metanolo ed etanolo. Tossicità del metanolo. Alcoli primari, secondari e terziari. I quattro alcoli C4. Struttura e proprietà fisiche. Punto di ebollizione e solubilità. Nomenclatura. Aldeidi e chetoni. Natura del gruppo carbonilico. Nomenclatura. Acidi carbossilici. Proprietà e nomenclatura. Esteri.
Esercitazioni: Gli odori delle molecole organiche: Etanolo, acetaldeide, acido acetico. Esteri. Solfossidi e ammine. Software ACDLabs: nomenclatura. Molecole contenenti più gruppi funzionali. Priorità.
Vedi Anche:
http://fco0809.blogspot.com/2009/03/lezione-del-18-marzo-2009.html
------------------------------------------------------------------------------------------------------
Esercitazioni: Gli odori delle molecole organiche: Etanolo, acetaldeide, acido acetico. Esteri. Solfossidi e ammine. Software ACDLabs: nomenclatura. Molecole contenenti più gruppi funzionali. Priorità.
Vedi Anche:
http://fco0809.blogspot.com/2009/03/lezione-del-18-marzo-2009.html
------------------------------------------------------------------------------------------------------
- Si avvisano gli studenti che informazioni e chiarimenti possono essere chieste inviando una e-mail a luilongo@gmail.com
- Si ricorda inoltre che gli studenti si ricevono presso il mio studio a MSA (Dipartimento di Scienze Chimiche, 0Mb-14 oppure Lab 0Mc-01, tel: 081674115 oppure 081674101) il mercoledì dalle 10 alle 12. Eccezionalmente, durante lo svolgimento del corso (5 marzo-20 maggio), gli studenti possono essere ricevuti anche il venerdì, sempre dalle 10 alle 12.
12 mar 2012
Lezione del 12 marzo 2012
Formule di Lewis. Cariche Formali. Carbonio: Ibridazione sp2. Ibridazione e geometria molecolare. Geometria trigonale planare. Alcheni. Nomenclatura. Ibridazione sp. Alchini. Geometria lineare. Stereoisomeria. 1 e 2-buteni. Isomeri geometrici E/Z. Idrocarburi con più doppi legami. Dieni.
Vedi anche:
http://fco0809.blogspot.com/2009/03/lezione-del-17-marzo-2009.html
Vedi anche:
http://fco0809.blogspot.com/2009/03/lezione-del-17-marzo-2009.html
6 mar 2012
Lezione del 5 marzo 2012
Lezione del 6 marzo
Introduzione alla Chimica Organica.
Il mondo fisico. Scale. Le dimensioni degli oggetti intorno a noi. Elettroni e Protoni. Atomi. Isotopi. La tavola periodica. Molecole. Punti di ebollizione di vari composti con l'idrogeno. L'acqua liquida!
vedi anche :http://fco0809.blogspot.it/2011/03/lezione-del-15-marzo-2011.html
vedi anche :http://fco0809.blogspot.it/2011/03/lezione-del-15-marzo-2011.html
Gli atomi del 1 e 2° periodo. Configurazioni elettroniche. Potenziale di ionizzazione e affinità elettronica. Elettronegatività. Il legame tra gli atomi. Legami ionici e covalenti. Polarizzazione dei legami covalenti. Il Carbonio. La molecola del metano. Discrepanza tra la configurazione del carbonio nel suo stato fondamentale e la presenza di quattro legami covalenti equivalenti. Ibridazione sp3. Gli Alcani. Butano. L'emergere della isomeria strutturale. Isobutano. Grafica Molecolare. Software ACDLabs. Visualizzazione delle molecole in 3D. La necessita di assegnare un nome alle molecole. Cicloalcani. 1,2-Dimetilciclopropani. L'emergere della Stereoisomeria.
17 gen 2012
3 gen 2012
Presentazione del corso
Corso di Laurea
|
Viticoltura ed Enologia
| |||||||||
Denominazione del corso
|
Chimica Organica
|
CFU: 9
| ||||||||
Docente
|
Luigi Longobardo
| |||||||||
Attività frontale(ore):
|
Lezioni teoriche
| 40 | ||||||||
Esercitazioni numeriche
| 30 | |||||||||
Laboratorio
|
-
| |||||||||
Seminari di approfondimento
|
-
| |||||||||
Studio individuale(ore):
|
Lezioni teoriche
|
100
| ||||||||
Esercitazioni numeriche
|
50
| |||||||||
Laboratorio
|
-
| |||||||||
Seminari di approfondimento
|
-
| |||||||||
Obiettivi formativi :
Il corso si prefigge di fornire le basi conoscitive della moderna teoria strutturale delle molecole organiche, al fine di favorire la lettura e la comprensione della diversità molecolare presente in natura, ma anche di quella derivante dalle trasformazioni chimiche ed enzimatiche delle più diffuse molecole naturali. In particolare rilievo la complessa relazione tra la struttura molecolare e le proprietà chimico-fisiche e biologiche delle sostanze.
| ||||||||||
Sintesi dei contenuti del programma:
Introduzione alla chimica organica. Gli atomi, il carbonio, le molecole. Orbitali, legami, ibridazione. Orbitali molecolari. Formule di Lewis. La risonanza. Idrocarburi saturi ed insaturi. Gruppi funzionali e classi di composti organici. Utilizzo di un Software in Chimica Organica. Grafica molecolare. Isomeria strutturale. La necessità di assegnare un nome alle molecole.
Stereoisomeria. Conformazioni e configurazioni. Simmetria molecolare. Geometria E/Z e cis-trans. Enantiomeri e diastereoisomeri. Stereochimica assoluta e relativa. Descrittori stereochimici R e S. Proiezioni di Fischer. Serie steriche D e L. Molecole con uno e più centri chirali. Esistenza fisica e realtà molecolare. Relazioni struttura-proprietà. Gli odori delle molecole organiche.
Chimica degli alcheni. Reazioni di addizione. Dieni. Aromaticità e composti aromatici. Fenoli e polifenoli. Acidità e basicità in chimica organica. Separazione di una miscela di sostanze organiche. Ossidazione delle molecole organiche. Processi ionici e radicalici.
Aldeidi e chetoni. Chimica del gruppo carbonilico. Formazione di acetali, cianidrine e reazioni con ammine. Enoli ed enolati. Condensazioni aldoliche. Fotosintesi. Monosaccaridi e polisaccaridi. Glicosidi. Ammine. Acidi carbossilici e derivati. Acidi lattico, succinico, malico e tartarico. Esteri e lattoni. Ammidi. Amminoacidi, peptidi e proteine. Nucleosidi e acidi nucleici. Lipidi e Terpeni.
| ||||||||||
Modalità di verifica dell'apprendimento:
Esame scritto e orale
| ||||||||||
Bibliografia: - - - - - - - - - - - - - - - - - - - - - - - -
· Software ACD/ChemSketch(Freeware):
| ||||||||||
14 dic 2011
Esami
Il prossimo appello di Fondamenti di Chimica Organica si terrà lunedì 16 gennaio 2012 ad Avellino alle ore 9.30 (unica data di gennaio).
Occorre prenotarsi via ESIS esattamente per la data indicata.
Occorre prenotarsi via ESIS esattamente per la data indicata.
30 ago 2011
Esami
Il prossimo appello è previsto per giovedì 22 settembre 2011 ad Avellino alle 9.30.
Occorre prenotarsi via ESIS per la data disponibile più vicina.
Iscriviti a:
Commenti (Atom)