Il prossimo appello è fissato per mercoledì 22 settembre 2010 alle ore 9.
Occorre prenotarsi via ESIS entro il 16 settembre

AAC – AMINO ACIDS CHEMISTRY DEPARTMENT OF CHEMICAL SCIENCES AT UNINA Dr. Luigi Longobardo • Room 2N19; Lab 2N18ab; • phone +39-081-674115; • Email: luilongo@unina.it; luilongo@gmai.com • orcid • webdocenti • Group website: http://fco0809.blogspot.it/ Research: Asymmetric synthesis Synthetic manipulation of α-amino acids. Sulfur and selenium-containing unnatural amino acids. Chemistry of Hydroxycinnamic Acids.
2 set 2010
29 giu 2010
Esame scritto del 28 Giugno 2010
Università degli Studi di Napoli Federico II
Scritto di Fondamenti Chimica Organica
28 Giugno 2010
|
1. Scrivere le strutture di Lewis delle molecole di seguito indicate, contenenti tutte un solo atomo di carbonio. Indicarne la sua ibridazione e la geometria molecolare osservata: a) anidride carbonica; b) metanolo; c) metanale; d) acido metanoico; e) metilammina; f) metanammide.
2. Scrivere la struttura delle molecole di seguito elencate, indicando per ognuna la classe di appartenenza e il numero di stereoisomeri possibili:
a) 2,3-butandiolo; b) 3,4-dicloro-4-(3,5-diidrossifenil)butan-2-one; c) acido 3-etil-5-idrossi-2-octenoico; d) 2-amino-3-idrossibutanamide; e) 2,3,4-triidrossibutanale; f) acido 2-amino-3-idrossibutandioico.
a) 2,3-butandiolo; b) 3,4-dicloro-4-(3,5-diidrossifenil)butan-2-one; c) acido 3-etil-5-idrossi-2-octenoico; d) 2-amino-3-idrossibutanamide; e) 2,3,4-triidrossibutanale; f) acido 2-amino-3-idrossibutandioico.
3. Il punto isoelettrico della glicina è 6. In che forma la troviamo a questo pH?
a) Qual è la forma prevalente allo stesso pH dell'acido acetico, della etilammina, dell'acetammide e dell’etanolo? b) Spiegare brevemente perché un'ammina è basica mentre una ammide è neutra; c) C'è una relazione tra la risposta data in b) e l'esistenza delle proteine?
a) Qual è la forma prevalente allo stesso pH dell'acido acetico, della etilammina, dell'acetammide e dell’etanolo? b) Spiegare brevemente perché un'ammina è basica mentre una ammide è neutra; c) C'è una relazione tra la risposta data in b) e l'esistenza delle proteine?
4. Dare una spiegazione ai seguenti fatti sperimentali: a) Il benzene da reazione di sostituzione elettrofila e non di addizione; b) Posto in un solvente polare il 3-clorociclopropene si dissocia in un carbocatione e lo ione cloruro; c) La piridina e il pirrolo sono entrambe aromatiche ma solo la piridina è basica; d) l’1,3-ciclopentadiene ha un pKa di 15.
5. Proporre, con un esempio, la struttura delle molecole di seguito classificate:
a) un L-deossialdoesoso; b) un D-chetopentoso; c) un L-a-amminoacido a pH 2;
d) un lipide idrolizzabile; e) una base pirimidinica presente nel RNA;
f) un generico dipeptide formato da D-a-amminoacidi.
a) un L-deossialdoesoso; b) un D-chetopentoso; c) un L-a-amminoacido a pH 2;
d) un lipide idrolizzabile; e) una base pirimidinica presente nel RNA;
f) un generico dipeptide formato da D-a-amminoacidi.
22 giu 2010
Esame scritto del 7 giugno 2010
1. Alla formula molecolare C4H8O2 corrispondono molecole appartenenti a varie classi. Suggerire il maggior numero di strutture possibili, assegnando ad ognuna la classe di appartenenza e il nome IUPAC.
2. Scrivere la struttura delle molecole di seguito elencate, indicando per ognuna la classe di appartenenza e il numero di stereoisomeri possibili: a) 2,3-diclorobutano; b) 3-(3-bromofenil)-3-idrossipropanale; c) acido 3-metil-2-esenoico; d) 3,4-diidrossipentanammide e) 2,3-dimetil-g-butirrolattone; f) 4,5-difeniloctan-3,6-dione.
3. Scrivere le strutture dei seguenti polifenoli, presenti prevalentemente nei vini rossi:
a) acido 2,4-diidrossibenzoico; b) acido 3,4,5-triidrossibenzoico; c) acido 3-idrossi-5-metossibenzoico; d) acido (2E)-3-(4-idrossifenil)prop-2-enoico; e) acido (2E)-3-(3,4-diidrossifenil)prop-2-enoico; f) acido (2E)-3-(4-idrossi-3-metossifenil)prop-2-enoico.
a) acido 2,4-diidrossibenzoico; b) acido 3,4,5-triidrossibenzoico; c) acido 3-idrossi-5-metossibenzoico; d) acido (2E)-3-(4-idrossifenil)prop-2-enoico; e) acido (2E)-3-(3,4-diidrossifenil)prop-2-enoico; f) acido (2E)-3-(4-idrossi-3-metossifenil)prop-2-enoico.
4. Dare una spiegazione delle seguenti osservazioni sperimentali: a) l’acido acetico ha un pKa = 5, mentre l’etanolo ha un pKa = 16; b) l’acido acetico ha un pKa = 5 mentre l’acido tricloroacetico ha un pKa = 1; c) il fenolo ha un pKa = 10 mentre il cicloesanolo ha un pKa = 16 ; d) perchè la etilammina è una sostanza basica con un pKb = 4, mentre l’acetammide è una sostanza neutra?
5. Proporre, con un esempio, la struttura delle molecole di seguito classificate:
a) un L-deossi aldopentososo; b) un D-chetoesoso; c) un D-a-aminoacido a pH 10; d) un lipide idrolizzabile; e) una base pirimidinica presente nel DNA; f) quanti sono i tripeptidi possibili utilizzando 3 a-amminoacidi racemi?
a) un L-deossi aldopentososo; b) un D-chetoesoso; c) un D-a-aminoacido a pH 10; d) un lipide idrolizzabile; e) una base pirimidinica presente nel DNA; f) quanti sono i tripeptidi possibili utilizzando 3 a-amminoacidi racemi?
Tempo a disposizione 2h. Si considera superata la prova con almeno 3 esercizi risolti
3 mag 2010
Purine + Pirimidine ed acidi nucleici
Nucleosidi, nucleotidi ed acidi nucleici
Dettagli possono essere trovati al link:
26 apr 2010
Lipidi
Lipidi e terpeni
Le sostanze grasse. Classificazione in base alle proprietà fisiche e non in base alla presenza di particolari gruppi funzionali. Lipidi idrolizzabili: cere, trigliceridi e fosfolipidi. Lipidi non idrolizzabili: vitamine liposolubili, eicosanoidi, terpeni e steroidi. Alimentazione e Salute. La dieta mediterranea e quella anglossasone!
Per ulteriori dettagli vedi:
21 apr 2010
Amminoacidi, peptidi e proteine
Amminoacidi, peptidi e proteine
Cenni sulla formazione prebiotica degli amminoacidi. Necessità di condizioni di asimmetria (chiralità) nella loro formazione. Il mondo L. Sterochimica degli amminoacidi. Proprietà acido-base. Il legame ammidico. Peptidi, proteine. Evoluzione chimica ed evoluzione biologica. Mondi reali e mondi possibili.
Per ulteriori dettagli vedi:
Carboidrati II
Carboidrati II
Formazione di emiacetali e acetali. Rappresentazione con le formule di Haworth e a sedia dei carboidrati. O-Glicosidi. Mutarotazione. Disaccaridi: Saccarosio, Maltosio, Lattosio e Cellobiosio. Polisaccaridi: Cellulosa e amido. La differenza tra uomini e mucche nel reperire il D-glucosio.
I colori del mondo naturale: Antocianine e loro glicoconiugati.

I colori del mondo naturale: Antocianine e loro glicoconiugati.

Per ulteriori dettagli vedi:
http://fco0809.blogspot.com/2009/05/lezione-del-28-aprile-2009.html
Separazioni di miscele di sostanze organiche
Separazioni di miscele di sostanze organiche sfruttando le loro proprietà acido-base. Cenni di cromatografia.
per ulteriori dettagli vedi:
http://fco0809.blogspot.com/2009/04/lezione-del-21-aprile-2009.html
per ulteriori dettagli vedi:
http://fco0809.blogspot.com/2009/04/lezione-del-21-aprile-2009.html
14 apr 2010
Carboidrati I
Carboidrati I
Il ciclo del carbonio. Cenni di fotosintesi clorofilliana. idrati di Carbonio, Cn(H2O)n. Il gruppo carbonilico. Fattori governanti la reattività. Reazioni tra composti carbonolici ed alcoli: formazione di emiacetali.
Per ulteriori dettagli vedi: Acetali e Carboidrati I
http://fco0809.blogspot.com/2009/04/lezione-del-22-aprile-2009.html
http://fco0809.blogspot.com/2009/04/lezione-del-22-aprile-2009.html
31 mar 2010
Acidi, Esteri e Lattoni
Acidi, Esteri e Lattoni.
Derivati degli acidi carbossilici
I principali acidi mono-, bi-, e tricarbossilici presenti nei vini:
Lattoni:
Quando la funzione alcolica è essa stessa presente nella struttura dell'acido carbossilico si forma un estere ciclico, che prende il nome di lattone:
Per una discussione generale sul "wine Lacton" vedi:
http://fco0809.blogspot.com/2009/05/lezione-del-6-maggio-2009.htmlDerivati degli acidi carbossilici:
Si definiscono derivati degli acidi carbossilici tutte quelle sostanze che per idrolisi (reazioni con H2O, catalizzate da acidi o basi) forniscono i corrispondenti acidi carbossilici. Tra essi, gli alogenuri acilici e le anidridi sono troppo reattive e pertanto non si trovano in natura. A differenza degli alogenuri alchilici, dove l'atomo di alogeno è legato ad un carbonio sp3, negli alogenuri acilici l'alogeno è legato direttamente al carbonio carbonilico ibridato sp2:
Aromaticità e composti aromatici
Aromaticità e composti aromatici
Per una discussione generale sulla aromaticità vedi nell'archivio aprile 2009
25 mar 2010
Enantiomeri e diastereoisomeri
Una datazione al carbonio 14 per le annate del vino
Dal sito de le Scienze
HTTP://LESCIENZE.ESPRESSO.REPUBBLICA.IT/ARTICOLO/ARTICOLO/1342550
HTTP://LESCIENZE.ESPRESSO.REPUBBLICA.IT/ARTICOLO/ARTICOLO/1342550
CHIMICA
Convegno dell’American Chemical Society
Una datazione al carbonio 14 per le annate del vino
Il metodo si basa sulla misurazione degli isotopi del carbonio contenuto nel vino: l'abbondanza relativa è stata alterata dagli esperimenti nucleari in atmosfera ammessi fino al 1963
24 mar 2010
Introduzione alla stereochimica
Introduzione alla Stereochimica
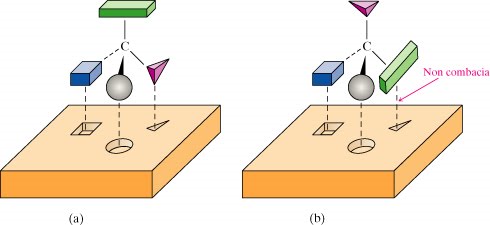
Dalla isomeria strutturale alla stereoisomeria. L'acido tartarico e la nascita della stereochimica. Il lavoro di L. Pasteur. Oggetti chirali e oggetti non chirali. Gli oggetti chirali hanno una immagine speculare che non è sovrapponibile all'oggetto originale.
L'atomo di carbonio asimmetrico. Elementi di simmetria molecolare. Assi e piani di simmetria. Gli stereoisomeri dell'acido tartarico. Enantiomeri e diastereoisomeri. Le mesoforme.
Come si distinguono 2 enantiomeri? La luce polarizzata. Polarizzatore. Misure di potere ottico rotatorio. Interazioni degli enantiomeri con altre sostanze chirali. Primi esempi di relazione struttura-proprietà.
La soluzione al grande enigma della Chimica Organica
I recettori biologici sono chirali. Interazione di due enantiomeri con un recettore biologico. Le proprietà odorose del limonene. Arancio e limone. Stereochimica assoluta. Attribuzione della configurazione assoluta a un atomo di carbonio asimmetrico.
Descrittori stereochimici R e S.
Descrittori stereochimici R e S.
Vedi anche Stereochimica I e Stereochimica II
http://fco0809.blogspot.com/2009/04/lezione-del-31-marzo-2009.html
http://fco0809.blogspot.com/2009/04/lezione-del-1-aprile-2009.html
17 mar 2010
Nomenclatura
Nomenclatura
La necessità di attribuire un nome alle molecole. Utilizzo del software ACDlab.
Primi esempi: geometria E-Z negli alcheni
Ulteriori esempi:
Acidità e basicità delle molecole organiche. Una introduzione. Comparazione tra l'acidità dell'acido acetico e dell'alcol etilico. Il ruolo della termodinamica e della cinetica nei processi chimici. Le reazioni acido-base.
Introduzione alla risonanza.
Composti ciclici. Ciclopropano, ciclobutano, ciclopentano, cicloesano.
Isomeria cis-trans nei 1,2-dimetilciclopropani
Ibridazione dell'atomo di carbonio e gruppi funzionali
Ibridazione
Configurazione elettronica del carbonio. La struttura e la forma del metano. Indistinguibilità dei legami C-H nel metano. Formazione di orbitali ibridi a partire dagli orbitali atomici. Ibridazione sp3. Geometria tetraedrica. Alcani. Ibridazione sp2. Formazione dei legami sigma e pi-greca. Geometria planare dell'etilene. Alcheni superiori. Ibridazione sp. Alchini. Gruppi funzionali. Alcoli, eteri, aldeidi, chetoni, acidi carbossilici, ammine, ammidi. Introduzione alla nomenclatura delle molecole organiche.
vedi anche http://fco0809.blogspot.com/2009/03/lezione-del-17-marzo-2009.html
10 mar 2010
Molecole
Molecole
Molecole organiche ed inorganiche. I principali atomi che si incontrano nella Chimica Organica. Idrogeno, ossigeno, azoto e carbonio. La formazione dei legami chimici. La molecola di H2. Orbitali atomici e molecolari. Isotopi dell'ossigeno. Ossigeno molecolare. Ammoniaca. Carbonio. Isotopi. Ossido e anidride carbonica. Metano. Idrocarburi. Reazioni di combustione con l'ossigeno. Formule molecolari e formule di struttura. Introduzione alla isomeria strutturale. Primi esempi: C2H4O2 e C3H6O2.
Introduzione alla Chimica Organica
Introduzione alla Chimica Organica
Tutte le rappresentazioni molecolari, incluse la discussione sulle proprietà periodiche degli elementi, sono generate usando il software ACD/ChemSketch versione 12.0 Freeware, scaricabile all'indirizzo http://www.acdlabs.com/download/chemsketch/
La tavola periodica. Elementi ed atomi. Il nucleo atomico. Cenni di nucleosintesi. Fusione e fissione atomica. Isotopi. Isotopi dell'uranio. Le proprietà periodiche degli elementi. Potenziale di ionizzazione, affinità elettronica ed elettronegatività. Atomi e molecole. Cenni di meccanica quantistica. Funzione d'onda. Configurazione elettronica. Legami covalenti e legami ionici.
17 nov 2009
Iscriviti a:
Commenti (Atom)